| 所属 |
① 京都大学 高等研究院 ヒト生物学高等研究拠点 (ASHBi) ② 京都大学 iPS細胞研究所 (CiRA)/ヒト生物学高等研究拠点 (ASHBi) |
|
|---|---|---|
| 氏名 |
① 辻村 太郎 ② 山本 拓也 |
|
| AMED 事業 |
課題名 | ロングリード1分子エピゲノム解析の支援 |
| 代表機関 | 京都大学 | |
| 代表者 | 辻村 太郎 | |
ロングリードシーケンサー、エピゲノム解析、クロマチン高次構造、アイソフォーム、DNAメチル化
エピゲノム解析はゲノム機能の発現制御機構を明らかにするために必須の技術である。ショートリード型の次世代シーケンス (NGS) 技術は、目覚ましい進歩を遂げながら、エピゲノム解析を牽引してきた。一方で、それらショートリードによる解析の限界も指摘されている。ショートリード解析では1DNA分子あたりせいぜい300bp長の断片化された形でしかエピゲノム情報をとらえられない。しかしながら、本来ゲノムは、kb~Mbの長さの単位スケールで機能する。例えば、転写制御では、数十~百kb以上離れた位置にあるエンハンサーと遺伝子プロモーターが相互作用する。このスケールのゲノム領域内では、~数百bpの単位で多種多様な領域がエピゲノム修飾を受けている。既存の技術では、これら複数ゲノム領域同士の活性の関連性や相互作用を1分子レベルで明らかにすることができない。近年発展してきたロングリードシーケンサーは、この既存技術の限界を突破する可能性をもつ。数十kb~Mb程度の1分子DNAの全長を連続的に解析できるため、長距離にわたるエピゲノム状態を1分子レベルで捉えることが可能になり、真に機能的な役割を果たすエピゲノム状態の解明に繋がる。本メニューでは、ロングリード解析技術を利用した以下の項目のエピゲノム解析を主に支援する。
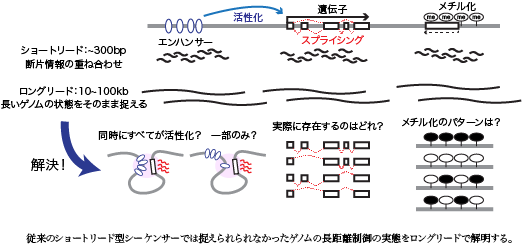
・クロマチン高次構造1分子マルチコンタクト解析
ゲノム中にある複数の制御領域が相互作用することで遺伝子の発現などが制御される。Hi-C法などの従来のショートリードシーケンスによるクロマチン高次構造解析手法では、1分子について原則1つのコンタクトペアしか捉えることができず、この複雑な相互作用の実態に迫ることは難しかった。本支援では、ロングリード技術を活用して複数領域間のコンタクトを同時に捉えることのできるクロマチン高次構造解析手法MC-3C/Pore-Cによる解析を支援する。
・1分子ロングリードメチローム解析
ロングリードシーケンサーによる、1分子DNAメチル化解析を支援する。
・全長mRNA解析
mRNAの直接解析、または全長cDNAライブラリーを作成してのアイソフォーム解析を支援する。
・その他ロングリードエピゲノム解析
要望に応じて、保有するロングリードシーケンサーを活用したエピゲノム解析を支援する。

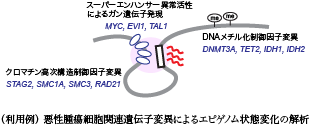
・ガン遺伝子の発現を誘導するスーパーエンハンサーの相互作用パターンの解析
・ダイナミックな発生過程における、分子レベルでのDNAメチル化パターンの変化の解析
・細胞種特異的なアイソフォームの同定
・1細胞全長トランスクリプトーム解析
京都大学高等研究院ASHBi単一細胞ゲノム情報解析コア (SignAC)
https://ashbi.kyoto-u.ac.jp/core-facility-ja/research-core-facility/sign-ac/
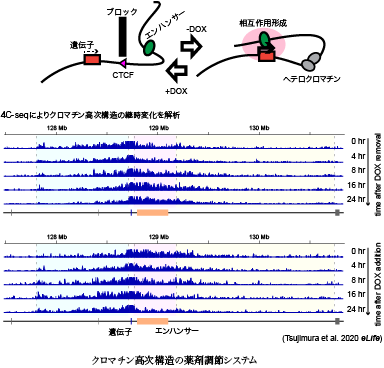
辻村は、ゲノム上に並ぶ遺伝子発現制御領域の機能解析をしてきた。特に、ゲノム工学およびエピゲノム解析の手法を活用して、複数の制御領域の間で起きる相互作用の形成機構の解明に取り組んできた。クロマチン高次構造とエンハンサーによる標的遺伝子活性化との関係を機能的に明らかにしてきたほか、その知見を応用して、薬剤でクロマチン高次構造と遺伝子発現を調節するシステムの開発を実現した。現在は、ロングリード技術を活用しながら、1分子レベル、シングルセルレベルでのエピゲノム制御の実態を明らかにすることを目的に研究に取り組んでいる。
山本は、遺伝子発現やエピジェネティックに関する網羅的データを解析することにより、細胞運命変換過程や細胞応答時における新規シグナル伝達経路を同定する手法の開発を行ってきた。例えば、数十のゲノム領域の染色体相互作用を高精度で同定できるms4C-seqを開発し、多能性幹細胞において発生関連遺伝子座は核の内部で集合しやすい傾向にあること、体細胞初期化過程において発生関連遺伝子座が再集合すること、それら遺伝子座の再集合にはエピジェネティック制御因子が必要であることを見出した。
https://www.cira.kyoto-u.ac.jp/ymt/