| 所属 |
① 理化学研究所 生命機能科学研究センター ② 大阪大学 大学院薬学研究科 |
|
|---|---|---|
| 氏名 |
① 本間 光貴 ② 福澤 薫 |
|
| AMED 事業 |
課題名 | AIとFMO法を融合したインシリコスクリーニングと分子間相互作用解析支援 |
| 代表機関 | 理化学研究所 | |
| 代表者 | 本間 光貴 | |
インシリコスクリーニング、AI、FMO
創薬ターゲットは、タンパク質の形状・性質に加え、活性化・阻害等の作用の違いなどがあり、異なる状況に応じて利用できるインシリコ創薬手法を準備しておく必要がある。当研究室では、ターゲットタンパク研究プログラム、創薬等支援プラットフォーム、先行のBINDSの3プロジェクトにおいて、各種のインシリコ創薬用システム(PALLAS, MUSES, LAILAPS)、FMO-PBSAによる活性予測手法を開発した。(下図)
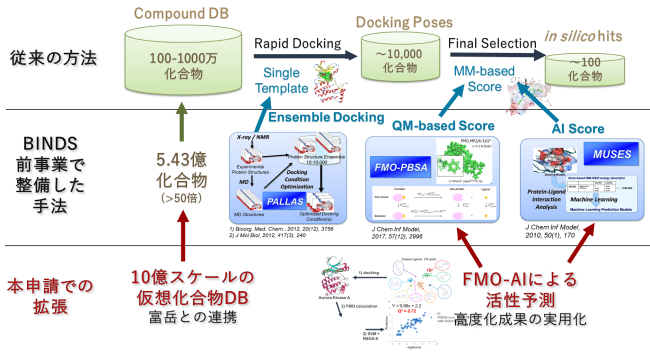
PALLASは、タンパク質構造の自由度、ドッキングの設定、アルゴリズムの中から最適な結果を与える条件を半自動的に探索するシステムであり、インシリコスクリーニングを行う際に無くてはならないものとなっている。得られたドッキングモデルの相互作用を解析し、AI活性予測を行うシステムがMUSESである。また、LAILAPSは、リガンド情報のみに基づく検索を行うシステムであり、部分構造検索、2D/3D類似検索、2D/3D記述子によるAI予測を同時に実施することができる。FMO-PBSAは、先行BINDSにおいて新たに開発したFMO法を用いた活性予測方法であり、現在、AIと組み合わせた発展型も利用可能である。
さらに、AMED次世代創薬AI事業(DAIIA)において、製薬企業18社から提供を受けたデータに基づいてオンオフターゲット、薬物動態、毒性等の数百種類の予測AIと構造発生AIを組み合わせた「創薬AIプラットフォーム」を開発しており、新BINDSにてそのプラットフォームと連携することも可能である。(DAIIAの了承が必要)
PALLAS, MUSES, LAILAPS, FMO-AI活性予測の一つまたは複数を組み合わせてインシリコスクリーニング及び最適化設計支援を実施する。初回の依頼においては、ドッキング、類似検索、AI予測等によるインシリコスクリーニングを実施する。すでに一度インシリコスクリーニングを実施して有望な化合物を得ているか依頼者が有望化合物を提供できる場合には、その化合物と標的タンパク質の立体構造、構造活性相関情報等に基づいて、ドッキング、FMO法による解析、創薬AIプラットフォーム等を利用した活性向上や体内動態・安全性プロファイルの最適化設計を行う。
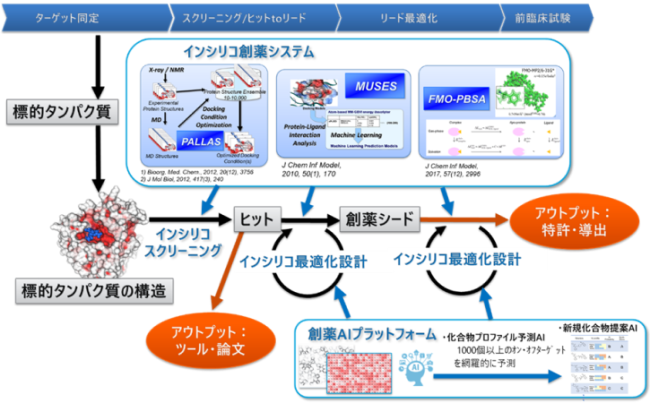
理化学研究所 生命機能科学研究センター及び大阪大学 大学院薬学研究科において、以上のインシリコ創薬システムを整備するとともに、実際のインシリコスクリーニングを実施できる研究スタッフを育成している。AMEDの先行プロジェクトや理研の創薬プロジェクトを通して、50以上の創薬ターゲットに対するインシリコスクリーニングに活用され、阻害剤・活性化剤の発見に貢献している。ヒットした化合物の最適化設計支援も実施し、動物モデルで薬効を示す化合物(AdipoR, HCK, ALK2, DOCK1/2, LSD1等)、10件以上の特許(うち国際出願5件)に結びついている。
https://www.bdr.riken.jp/ja/research/labs/honma-t/index.html
https://www.phs.osaka-u.ac.jp/research/researcherDetail.php?id=36