| 所属 |
① 九州大学 大学院薬学研究院 ② 九州大学 生体防御医学研究所 ③ 九州大学 大学院薬学研究院 |
|
|---|---|---|
| 氏名 |
① 真柳 浩太 ② 神田 大輔 ③ 松永 直哉 |
|
| AMED 事業 |
課題名 | グリーンファルマ創薬構造解析による支援高度化の推進 |
| 代表機関 | 九州大学 | |
| 代表者 | 大戸 茂弘 | |
急速凍結試料作製、クライオ電子顕微鏡、自動データ収集、単粒子解析、超分子複合体の立体構造解析
近年、検出器の発達及び革新的解析ツールの開発・普及に伴い、クライオ電子顕微鏡単粒子解析法を使った立体構造解析は飛躍的に分解能が向上した。九州大学薬学研究院はグリーンファルマ構造解析センターを設置し(令和4年4月1日)、2台の最新型のクライオ電顕(日本電子製)によるタンパク質超分子複合体の立体構造解析の支援を開始した。本装置が最新型の高性能電子顕微鏡であることから、振動、温度変化、磁場等の環境による影響を極力抑制して装置の性能を最大限に引き出すため、環境測定によりキャンパス内に適切な場所を選定し、専用の建物を設計・建設した。

九州大学薬学研究院では既存承認薬の適応拡大(育薬エコファーマ)と、地球環境にやさしい薬の合成(グリーンケミストリー)を融合させた「グリーンファルマ」を推進している。薬学研究院内の承認薬ライブラリーを用いたスクリーニング支援等から得られたヒット化合物と、ターゲットタンパク質との複合体等の立体構造を原子レベルで明らかにすることで創薬研究を加速する。
1) クライオ電子顕微鏡を用いた構造解析のコンサルティング
効率良く構造解析支援が進行するように、ターゲット等についての事前相談を行い。試料調製の方針等のコンサルティングを行う。サンプルの負染色法による事前チェックも可能である。
2)凍結試料作製
ユーザーが凍結済み試料を持ち込む場合と、来所後にセンター内の急速凍結装置(Vitrobot:下図)を用いて凍結する場合の2通りが可能。
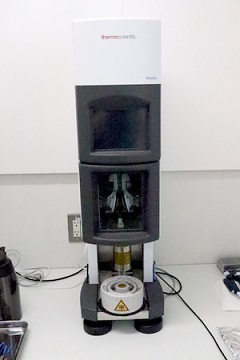
3)クライオ電子顕微鏡による観察、自動撮影セットアップ、観察スクリーニング実験
主にARM200を使用した自動撮影(条件設定等、サンプル選定、撮影箇所等)のセットアップを支援。
構造解析に適した試料調製、凍結条件、撮影条件等を検討する。
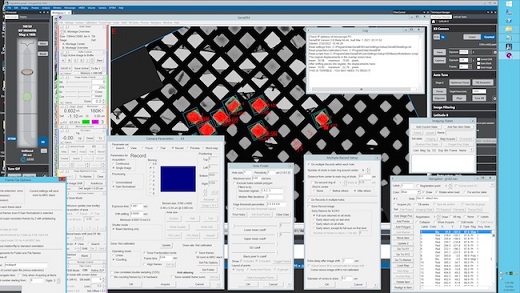
4)高分解能解析用データ収集
主にARM300IIを使用する。本顕微鏡はセットアップ時の動作確認測定にて、2Åを超える高分解能データの取得を確認している(図はアポフェリチンの1.6Åの密度マップ)。スクリーニングと同様、高分解能データの自動撮影のセットアップを支援する。
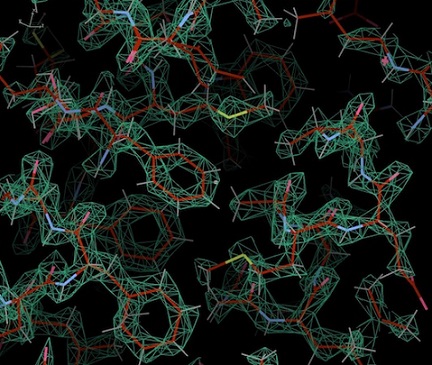
5)単粒子解析の支援
ユーザーが単粒子解析に必要な計算機等を所有していない場合、センター内のGPU計算機やスパコンITO(下図)を活用することにより、初期投資を抑えて必要な計算環境を提供。

6)創薬支援
九大薬学研究院のスクリーニング支援メニューによって得られたヒット化合物とターゲットタンパク質との複合体の構造解析を支援する。原子分解能の構造情報を使って阻害機構を原子レベルで解明することを通して創薬研究を加速する。
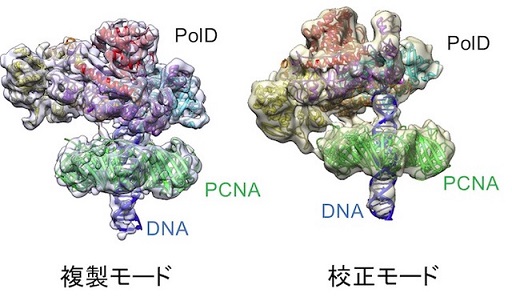
DNA複製複合体のクライオ電顕による解析
DNAの複製に関わる超分子複合体は柔軟な構造を持つ。また因子間の相互作用が天然変性領域を介して行われるため構造解析が困難なものが多い。DNA複製複合体を中心に解析を進め、複製因子の切り替え、各因子の機能モード(複製⇔校正)切り替えの制御機構等を明らかにした。
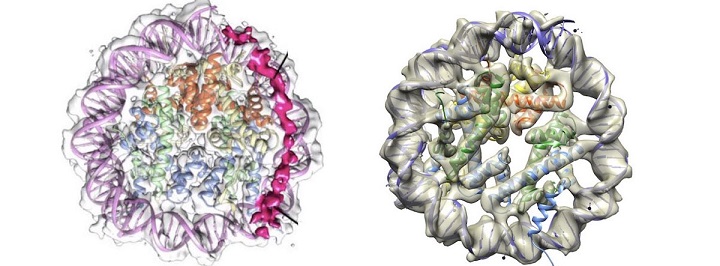
ヒストンシャペロンFACTによるヌクレオソーム構造の不安定化の機構の解明
1. 天然変性領域がDNAと入れ替わりヌクレオソームに侵入する不安定化の初期過程を可視化した(左)。
2. 8個のヒストンから2個が脱落した反応の生成物であるhexasomeの溶液中構造を可視化した(右)。