| 所属 |
① 大阪公立大学 研究推進機構/理学研究科 ② 大阪公立大学 研究推進機構/理学研究科 ③ 大阪公立大学 研究推進機構/理学研究科 |
|
|---|---|---|
| 氏名 |
① 藤井 郁雄 ② 藤原 大祐 ③ 道上 雅孝 |
|
| AMED 事業 |
課題名 | 分子標的中分子ペプチド創出の支援 |
| 代表機関 | 大阪公立大学 | |
| 代表者 | 藤井 郁雄 | |
ポスト抗体医薬、分子標的ペプチド、中分子創薬、立体構造規制ペプチド、細胞表層提示ライブラリー
支援先より提供される標的タンパク質(疾患関連タンパク質など)に対して、独自のHLHペプチド・ライブラリーをスクリーニングして標的タンパク質に作用する分子標的HLHペプチドを取得し、提供する(図1)。
このHLHペプチドは、ヘリックス・ループ・ヘリックス(HLH)構造をもつ立体構造規制ペプチドである。強固なヘリックス構造を保持していることから、標的タンパク質に対し強い結合活性と高い特異性をもち、タンパク質―タンパク質相互作用を阻害する。また、血中での酵素分解に対し高い安定性を示す。さらに、動物実験(マウス)により、免疫原性をもたないことを確認している。すなわち、分子標的HLHペプチドは、抗体と同等の結合活性と安定性をもっており、生物学的ツール及び医薬品としての有用性を持つ(図2)。

当研究グループでは、ポスト抗体医薬の候補分子として、ヘリックス―ループ―ヘリックス(HLH)構造モチーフをもつ立体構造規制ペプチド(分子標的HLHペプチド)を設計した。図3に示すように、このペプチドは3つの領域で構成されている、①N末端ヘリックス(14アミノ酸残基からなる構造支持領域)、②ループ(Gly 7残基からなるリンカー)、③C末端ヘリックス(14アミノ酸残基からなる相互作用領域)。2つのヘリックスは、内側に存在するLeu基(緑色)の疎水相互作用及び側面のGlu基(橙色)とLys基(青色)の静電相互作用により寄り添い、安定な構造を形成する。一方、ヘリックス外側のアミノ酸は立体構造構築に関わっていない。したがって、外側のアミノ酸(X部分:黄色)をさまざまなアミノ酸に置換することにより、HLH構造のペプチド・ライブラリーを構築することができる。このライブラリーを提示させ(ファージ表層提示ライブラリー)、各種標的タンパク質(疾患関連タンパク質)に対してスクリーニングし、強い結合活性をもつ分子標的HLHペプチドの獲得に成功している。
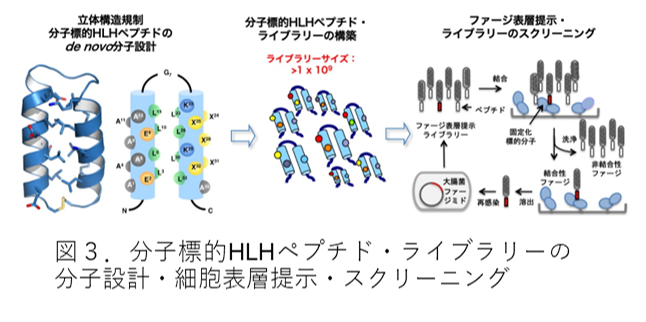
国内外において、非イムノグロブリン骨格の抗体様物質の研究が行われている。これらは、天然タンパク質を土台にして作製されているため、小さいものでも分子量が10,000を超え、その結果、免疫原性があり、また細胞膜透過性などの問題を残している。一方、分子標的HLHペプチドは、完全de noveで設計されており、そのため分子量を5000以下に抑えることに成功している。その結果、非免疫原性、細胞透過性を獲得し、また低コストでの化学合成が可能になるなど、多くの点で優れており、非常に独自性の高いものである。
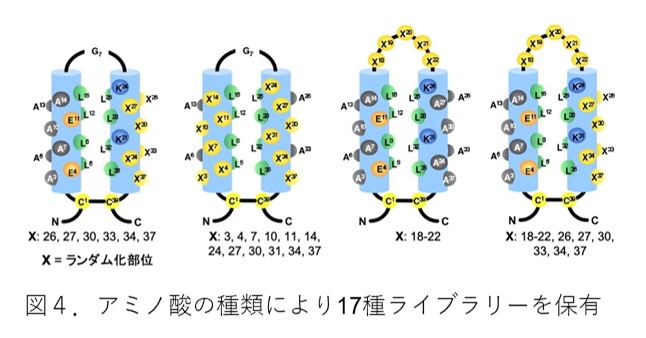
当研究グループでは、図4のような相互作用トポロジー(ランダム変異部位)の異なる4種の分子標的HLHペプチド・ライブラリーを構築し、またアミノ酸の種類の違いにより、17種のライブラリーを保有している(各ライブラリーサイズ>1x109)。また、分子標的HLHペプチドの酵母表層提示ライブラリーも構築している(図5)。酵母ライブラリーの場合、FACSによる1分子1細胞のスクリーニングが可能になり、効率約に分子標的ペプチドを獲得することができる。さらに、スクリーニング過程をNGSによりモニターすることで、分子標的ペプチドのヒット確率が格段に良くなる(図5)。

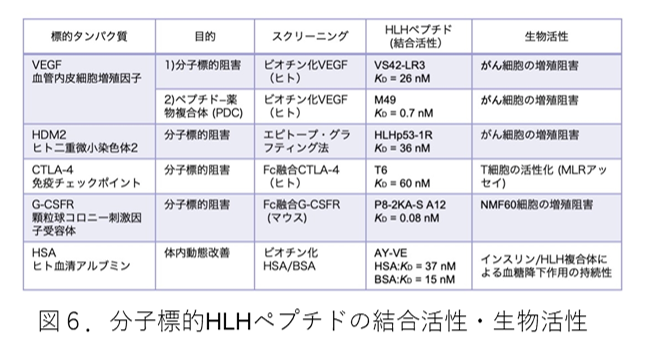
抗体様物質として、安定なヘリックス―ループ―ヘリックス構造をもつペプチド「分子標的HLHペプチド」の開発を行っている。進化分子工学的手法により、すでに、各種のサイトカインや受容体に対する分子標的ペプチドの獲得に成功している。図6に示すように、どの標的タンパク質に対しても、強い結合活性(KD= 10-8~10-11M)の分子標的ペプチドが得られている。顆粒球コロニー刺激因子(G-CSF)受容体の場合、獲得された分子標的HLHペプチドは、強い結合活性(Kd =0.08 nM)をもち、G-CSFによる細胞増殖を完全に阻害する(抗G-CSFRペプチド:Current Protocols in Chemical Biology 5, 171-194, 2013)。このペプチドは、強固なヘリックス構造を保持しており(helix 59%)、マウス血清を用いて酵素分解に対する安定性を経時的に追跡したところ、15日の半減期をもつことが判明した。さらに、マウスに免疫し、分子標的HLHペプチドが抗原性をもたないことを確認している(非免疫原性)。すなわち、分子標的HLHペプチドは、低分子量であるにもかかわらず抗体と同等の強力な結合活性(Kd:数nM以下)を示し、かつ酵素分解に対して高い安定性(血清中半減期:14日以上)をもち、非免疫原性であることから、従来の抗体医薬の問題点を一挙に解決し、これに代わりうる革新的医薬品開発につながる。
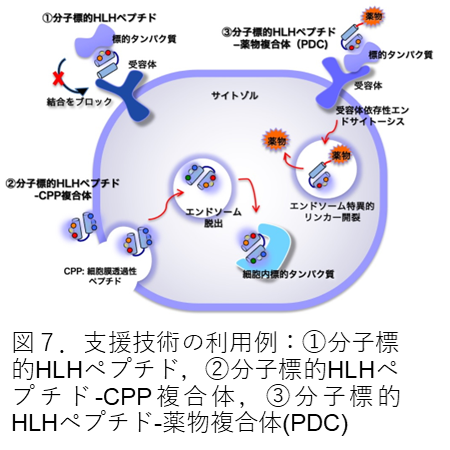
当研究グループでは、分子標的HLHペプチドとそれに関わる基盤技術を開発し、新しい創薬モダリティーの確立を目指している。支援技術の利用例として、作用メカニズムの異なる3つの分子標的HLHペプチドについて紹介する。図7に示す①分子標的HLHペプチドは、抗体医薬と同様に、標的タンパク質に結合し、受容体との相互作用を阻害してシグナル伝達を遮断する(抗CTLA4ペプチドなど: ACS Chem. Biol. 15, 360-368, 2020)。②分子標的HLHペプチド―CPP複合体は、CPP(細胞膜透過性ペプチド)の作用により細胞内に取り込まれ、その後エンドソームより放出され、細胞内の標的タンパク質に作用する(抗HDM2ペプチドなど: Angew. Chem. Int. Ed. 55, 10612-10615, 2016)。③分子標的HLHペプチド-薬物複合体(Peptide-Drug Conjugate:PDC)は、ペプチドにリンカーと呼ばれる部分を介して化学療法剤などの薬物を共有結合したものである(抗VEGFペプチド: PLoS ONE, 16(2): e0247045, 2021)。当グループでは、血管内皮細胞増殖因子(VEGF)などのがん細胞が活発に生産するタンパク質を標的にしている。PDC は、まずがん細胞周辺の標的タンパク質と結合し複合体を形成する。PDC は、抗体と異なり分子サイズが小さいので、標的タンパク質に結合しても、標的タンパク質と受容体との相互作用を阻害することはない。したがって、PDC―標的タンパク質―受容体の3量体を形成し、受容体依存性エンドサイトーシスを誘発して、細胞内に取り込まれる。その後、エンドソーム内でリンカーの開裂が起こり薬物を細胞内に放出する。
HLHペプチドの体内動態を改善するために、ヒト血清アルブミンに結合するペプチドを作製した(抗HSAペプチド: DOI: 10.1021/acs.molpharmaceut. 2c00106 )。本ペプチドとインスリンの複合体を作製したところ、インスリンの血糖降下作用を延長できることが判明した。本ペプチドのアミノ酸配列を分子標的HLHペプチドに移植することにより、体内動態の改善が可能になる。
“分子標的HLHペプチドを基盤とした新しい創薬モダリティーの開発”
21世紀に入るとともにヒトの遺伝子構造の全容が明らかにされた。現在、ゲノムから翻訳されるタンパク質の網羅的な解析が進められており、生命科学研究や医薬品開発の標的タンパク質が劇的に増えてきている。この急速なプロテオーム解析に迅速に対応するために、タンパク質-タンパク質相互作用を制御する分子標的化合物の新しい設計法が求められている。現在、タンパク質相互作用に対する分子標的ツールとして抗体が注目されており、また分子標的医薬品としても汎用されるようになってきている。しかし、抗体(抗体医薬)には、致命的な欠点があり、以下のような問題点が指摘されている(図8)。①抗体は,多数のジスルフィド結合を含む巨大タンパク質であるため、細胞内に導入したり、細胞内で機能させたりすることができず、細胞内の疾患関連タンパク質をターゲットとすることができない。②ヒトに対する抗原性を下げるため、ヒト化等が必要である。③モノクローナル抗体であるために生産に膨大なコストを必要とする。その結果として薬剤治療費が高騰し社会問題になっている。さらに、④抗体医薬の開発や生産には、特許の制限が複雑に絡み合っている。これらの問題点は全て、抗体の基本構造に起因するものである。そこで、本研究では、イムノグロブリン構造を利用せず、目的の標的タンパク質に対して特異的に結合する抗体様分子「分子標的HLHペプチド」の設計法を確立し、従来の抗体が抱える複数の課題をすべて克服する。今後、がん細胞を用いたin vitro評価、担がんマウスを用いたin vivo評価までを実施し、分子標的HLHペプチドによる抗がん治療の概念実証(Proof of Concept)を示し、分子標的HLHペプチドとそれに関わる基盤技術を、日本発信の新しい創薬モダリティーとする。